cooh.cc 高中有机化学资料库
高中有机化学【全部官能团】完整详解
以下涵盖高中教材所有要求掌握的官能团,按类别划分,结构、性质、特征反应、典型物质一目了然,是高考有机推断题的核心依据。
一、烃类官能团
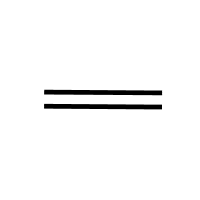
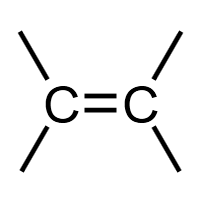
碳碳双键 (=C=C=):烯烃官能团,平面结构,键角约120°。可发生加成反应(与溴水、H₂、HX、H₂O等)、氧化反应(使酸性KMnO₄溶液褪色)、加聚反应。典型物质:乙烯、丙烯。

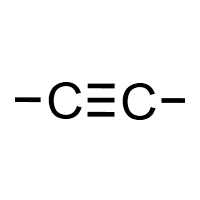
碳碳三键 (-C≡C-):炔烃官能团,直线结构,键角180°。化学性质比双键更活泼,可发生加成、氧化、聚合反应,能使溴水、酸性KMnO₄褪色。典型物质:乙炔、丙炔。
二、含氧官能团
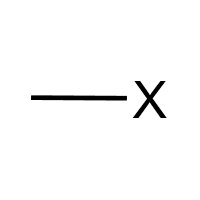
卤原子 (-X, F/Cl/Br/I):卤代烃官能团。可发生水解反应(取代,生成醇)、消去反应(生成不饱和键,要求邻位碳有H)。典型物质:溴乙烷、氯甲烷。
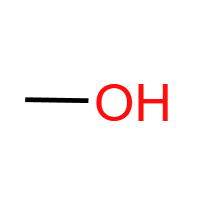
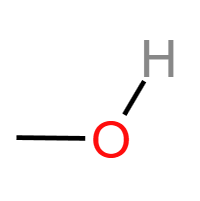
醇羟基 (-OH):醇类官能团。可与Na反应放H₂,可发生消去(邻位有H)、催化氧化(α-C有H,变醛/酮)、酯化反应。典型物质:乙醇、乙二醇。
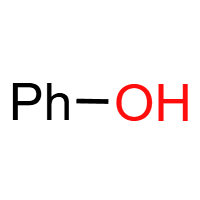
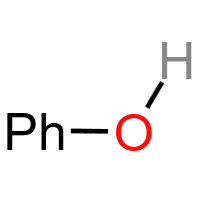
酚羟基 (-OH):酚类官能团(与苯环直接相连)。弱酸性(酸性弱于碳酸,强于HCO₃⁻),与溴水发生邻对位取代生成白色沉淀,遇FeCl₃溶液显紫色。典型物质:苯酚。(图片中Ph表示苯基)
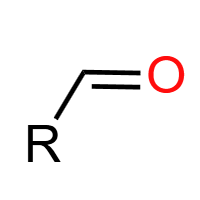
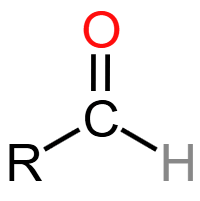
醛基 (-CHO):醛类官能团。强还原性,可发生银镜反应、与新制Cu(OH)₂悬浊液反应生成砖红色沉淀,可氧化为羧酸、还原为醇。典型物质:乙醛、甲醛。
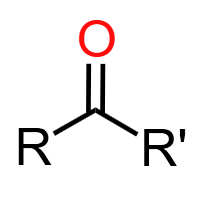
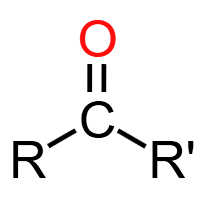
酮羰基 (>C=O):酮类官能团(与两个烃基相连)。可发生加成还原反应(生成醇),不能被银氨溶液、新制Cu(OH)₂氧化。典型物质:丙酮。
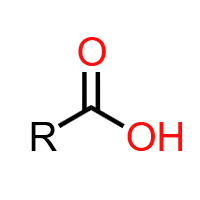
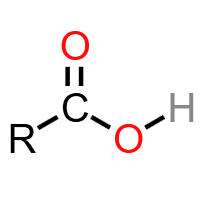
羧基 (-COOH):羧酸官能团。具有酸性(酸性强于碳酸),能与Na、NaOH、Na₂CO₃、NaHCO₃反应,可与醇发生酯化反应。典型物质:乙酸、苯甲酸。
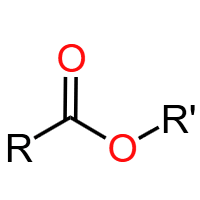
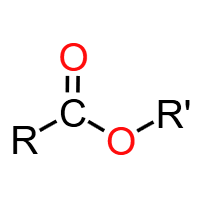
酯基 (-COO-):酯类官能团。难溶于水,密度比水小,可在酸性(可逆)或碱性(不可逆)条件下水解,生成酸和醇。典型物质:乙酸乙酯、油脂。
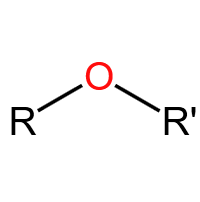
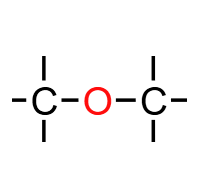
醚键 (-O-):醚类官能团。性质稳定,常温下不与钠、酸、碱反应,常用作有机溶剂。典型物质:乙醚、甲乙醚。
三、含氮/硫官能团
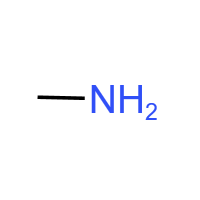
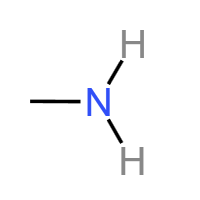
氨基 (-NH₂):胺类、氨基酸官能团(N原子链接3个单键就属于氨基)。具有碱性,能与酸反应生成盐,可与羧基发生类似酯化的反应形成肽键。典型物质:甲胺、甘氨酸。
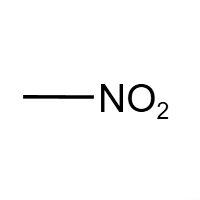
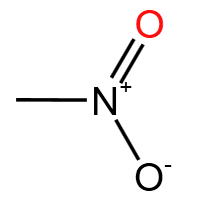
硝基 (-NO₂):硝基化合物官能团。可被还原为氨基,是制备染料、药物的重要中间体。典型物质:硝基苯。
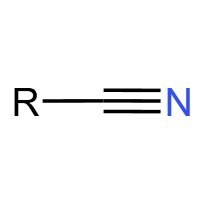
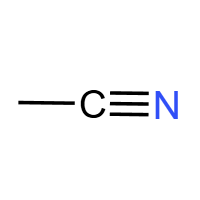
氰基 (-CN):腈类官能团。酸性水解生成羧酸,碱性水解生成羧酸盐,可用于有机合成增长碳链。典型物质:乙腈。
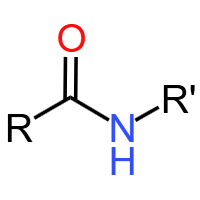
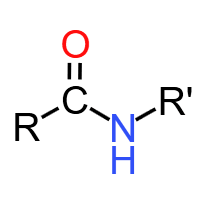
酰胺基(肽键) (-CONH-):蛋白质、酰胺官能团。由羧基与氨基脱水缩合(成肽反应)形成,可发生水解反应断裂,生成氨基酸。典型物质:二肽、蛋白质。
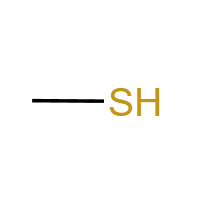
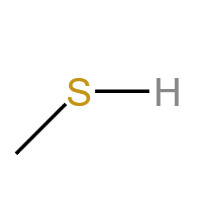
巯基 (-SH):硫醇官能团。具有还原性,易被氧化为二硫键,是蛋白质二级结构的重要组成,性质类似羟基。典型物质:半胱氨酸。
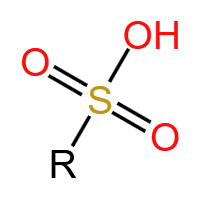
磺酸基 (-SO₃H):强酸性基团,由硫酸脱去羟基生成,水溶性极强,常见于染料、表面活性剂、磺酸类药物。典型物质:苯磺酸。
官能团性质核心总结
1. 能使酸性KMnO₄褪色的基团:碳碳双键、碳碳三键、醛基、醇羟基(α-C有H)、苯环侧链(与苯环相连的C有H)、酚羟基。
2. 能使溴水褪色的基团:碳碳双键、碳碳三键、醛基、酚羟基。
3. 能与Na反应的基团:醇羟基、酚羟基、羧基。
4. 能与NaOH反应的基团:酚羟基、羧基、酯基(水解)、卤原子(水解)。
5. 能与NaHCO₃反应的基团:仅羧基。